احتراق یکی از پدیدههای اساسی در تأمین انرژی مورد نیاز زندگی روزمره و صنایع مختلف بهشمار میرود. درک اصول بنیادی آن نهتنها ضروری، بلکه برای بهینهسازی و کنترل فرآیندهای احتراقی حیاتی است. شیمی، بهعنوان ستون این پدیده، زیربنای مفاهیم احتراق را تشکیل میدهد. بنابراین بررسی و برجسته کردن مفاهیم اساسی شیمی که در ادامه به آن پرداخته شده است، در بررسی فرآیند احتراق نقش کلیدی خواهند داشت.
فرآیند احتراق
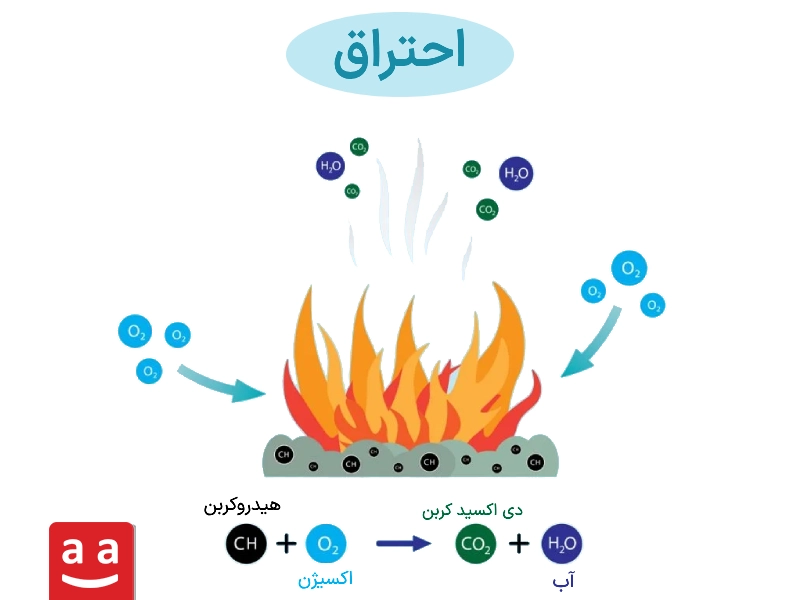
این فرایند عبارت از اکسیداسیون اجزایی از ترکیب سوخت است که قابلیت اکسید شدن دارند و میتوان آن را به صورت یک معادله شیمیایی بیان کرد. در طی فرآیند احتراق، جرم هر عنصر ثابت باقی خواهد ماند، بنابراین لازم است در تمامی واکنشها، قانون بقای جرم برقرار باشد. مطابق با معادله 1 سادهترین نوع واکنش، واکنشی است که بین کربن و اکسیژن صورت میگیرد.
معادله 1
C + O2 → CO2
معادله 1 بيان ميكند كه 12 کیلوگرم (معادل یک کیلو مول) کربن با 32 کیلوگرم (معادل یک کیلو مول) اکسیژن واکنش داده و 44 کیلوگرم (معادل یک کیلو مول) کربن دی اکسید بهدست میآید. اجزای شرکت کننده در واکنش احتراقی، واکنشدهنده و مواد حاصل از فرآیند سوختن، فرآورده نامیده میشوند. فرم کلی یک واکنش احتراق به صورت معادله 2 بیان میشود.
معادله 2
انرژی + نیتروژن + کربن دی اکسید + بخار آب → اکسید کننده + سوخت
در واکنشهای احتراقی، بخار آب و کربن دی اکسید محصولات اصلی واکنش هستند. بسته به درجه حرارت و فشار محصولات اشتعال، آب میتواند به صورت مایع یا بخار ظاهر شود. در اکثر موارد، به جای استفاده از اکسیژن خالص به عنوان اکسید کننده، از مقدارمعینی هوا استفاده میشود. ترکیب هوا در مبنای مولی شامل 21 درصد اکسیژن، 78 درصد نیتروژن، 1 درصد آرگون و گازهای دیگر است. در محاسبات احتراق به طور معمول آرگون و سایر گازها را در نظر نگرفته و فرض میشود که هوا از 21 درصد اکسیژن و 79 درصد نیتروژن بر مبنای مولی تشکیل شده است. با این فرض به ازای هر مول اکسیژن در هوا، 76/3 مول نیتروژن وجود دارد.
در مقالهی “ احتراق سوخت پاک ” توضیحات جامع و کاملی درباره سوختهای پاک ارائه شده است. برای کسب اطلاعات بیشتر، مطالعه این مقاله پیشنهاد میشود.
هوای نظری و اضافی
حداقل مقدار هوای لازم برای سوختن کامل سوخت، هوای نظری (تئوری) نامیده میشود. در طی یک واکنش با مقدار هوای نظری، در سمت فرآوردهها هیچگونه اکسیژنی وجود نخواهد داشت و میتوان واکنش را به صورت معادله 3 در نظر گرفت.
معادله 3
ضرایب استوکیومتریک موجود در معادله 3 را میتوان با استفاده از اصول موازنه بهدست آورد. این ضرایب در جدول 1 آورده شدهاند.
![Rendered by QuickLaTeX.com \[ \Large % تغییر سایز به بزرگتر \renewcommand{\arraystretch}{2} % افزایش فاصلهی عمودی برای وسطچین شدن متن \begin{array}{|c|c|} \hline \multicolumn{1}{|c|}{x + \frac{y}{4}} & \multicolumn{1}{c|}{v_{O_2}} \\ % وسطچین \hline \multicolumn{1}{|c|}{x} & \multicolumn{1}{c|}{v_{CO_2}} \\ % وسطچین \hline \multicolumn{1}{|c|}{\frac{y}{2}} & \multicolumn{1}{c|}{v_{H_2O}} \\ % وسطچین \hline \multicolumn{1}{|c|}{3.76\left(x + \frac{y}{4}\right)} & \multicolumn{1}{c|}{v_{N_2}} \\ % وسطچین \hline \end{array} \]](https://raadmanburner.com/fa/wp-content/ql-cache/quicklatex.com-264d5417fde2ab626eb820683851cbba_l3.png)
![Rendered by QuickLaTeX.com \[ \Large % تغییر سایز به بزرگتر \renewcommand{\arraystretch}{2} % افزایش فاصلهی عمودی برای وسطچین شدن متن \begin{array}{|c|c|} \hline \multicolumn{1}{|c|}{x + \frac{y}{4}} & \multicolumn{1}{c|}{v_{O_2}} \\ % وسطچین \hline \multicolumn{1}{|c|}{x} & \multicolumn{1}{c|}{v_{CO_2}} \\ % وسطچین \hline \multicolumn{1}{|c|}{\frac{y}{2}} & \multicolumn{1}{c|}{v_{H_2O}} \\ % وسطچین \hline \multicolumn{1}{|c|}{3.76\left(x + \frac{y}{4}\right)} & \multicolumn{1}{c|}{v_{N_2}} \\ % وسطچین \hline \end{array} \]](https://raadmanburner.com/fa/wp-content/ql-cache/quicklatex.com-264d5417fde2ab626eb820683851cbba_l3.png)
جدول 1 ضرایب استوکیومتریک واکنش احتراق
بنابراین برای سوختن کامل یک مول سوخت هیدروکربنی با فرمول شیمیایی مشخص شده در معادله 3 به مقدار (x+y/4)4.76 مول هوا نیاز است. این مقدار هوا معادل 100 درصد هوای نظری است. با این وجود در عمل، سوختن کامل هنگامی رخ میدهد که مقدار هوای تامین شده تا حدودی بیشتر از مقدار هوای نظری باشد. بنابراین به منظور تعیین میزان هوای اضافی مورد نیاز جهت احتراق، دو پارامتر AF و λ تعریف میشود. پارامتر AF نسبت هوا به سوخت بوده و مطابق معادله 4 و معادله 5 به ترتیب بر مبنای جرمی و مولی تعریف میشود.
معادله 4
![]()
![]()
معادله 5
![]()
![]()
نسبت هم ارزی ϕ مطابق با معادله 6 به صورت نسبت نظری هوا به سوخت تقسیم بر نسبت واقعی هوا به سوخت تعریف میشود.
معادله 6
![]()
![]()
در صورتی که ϕ<1 باشد مخلوط از نظر سوخت رقیق و احتراق دارای هوا اضافه است و در صورتی که ϕ>1 مخلوط از نظر سوخت غنی نامیده میشود. مقدار واقعی هوای بکار رفته را میتوان برحسب درصد هوای اضافه λ به صورت معادله 7 بیان کرد.
معادله 7
![]()
![]()
منظور از زیر نویس s، مقدار پارامتر در حالت استوکیومتری است. استفاده از 20 % هوای اضافی (%λ=20) در احتراق صنعتی رایج است.
آلایندههای حاصل از اشتعال
همانطور که گفته شد در صنعت، سوختن کامل هنگامی رخ میدهد که مقدار هوای تامین شده تا حدودی بیشتر از مقدار هوای نظری باشد. در صورت بروز سوختن ناقص، محصولات جانبی به عنوان آلایندههای احتراق تولید میگردند. از مهمترین و مورد توجهترین آلایندههای اشتعال، کربن مونوکسید و ناکس هستند. با تنظیم میزان هوای اضافی، میتوان آلایندههای ناشی از سوختن را کنترل نمود. در شکل زیر میزان تولید آلایندههای کربن مونوکسید و ناکس بر حسب نسبت هوا به سوخت در یک فرآیند احتراقی نشان داده شده است.
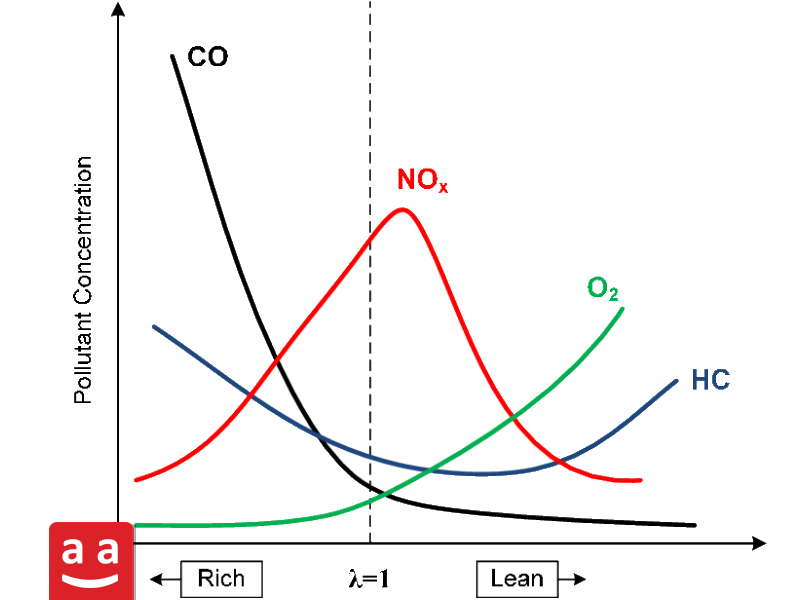

میزان تولید ناکس در نزدیکی نسبت هوا به سوخت استوکیومتری در حالت بیشینه است و با کاهش نسبت هوا به سوخت، تولید آلاینده ناکس کاهش مییابد در این حالت، انتشار کربن مونوکسید افزایش یافته است. با افزایش هوای اضافی نسبت به هوای استوکیومتری، انتشار آلایندههای کربن مونوکسید و ناکس به طور همزمان، کاهش خواهد یافت، با این حال با افزایش بیش از حد این نسبت، از یک سو دمای شعله کاهش یافته و از سوی دیگر اتلافات دودکش افزایش مییابد. این دو در مجموع موجب کاهش راندمان سوختن میشوند. لذا همواره در هر فرآیند احتراقی میزان هوای اضافی بهینهای باید لحاظ گردد.
آلایندگی ناشی از نیتروژن
حضور اکسیدهای نیتروژن در جو به تشکیل مهدود، باران اسیدی، گرم شدن کره زمین و تخریب لایه ازون کمک خواهد کرد. منبع اصلی تولید اکسیدهای نیتروژن، احتراق سوختهای فسیلی در کورهها و موتورهای احتراقی است. مهمترین ترکیبات اکسیدهای نیتروژن نیتروژن مونوکسید (NO) ، نیتروژن دیاکسید ( NO2 ) و نیتروز اکسید (N2O) است.
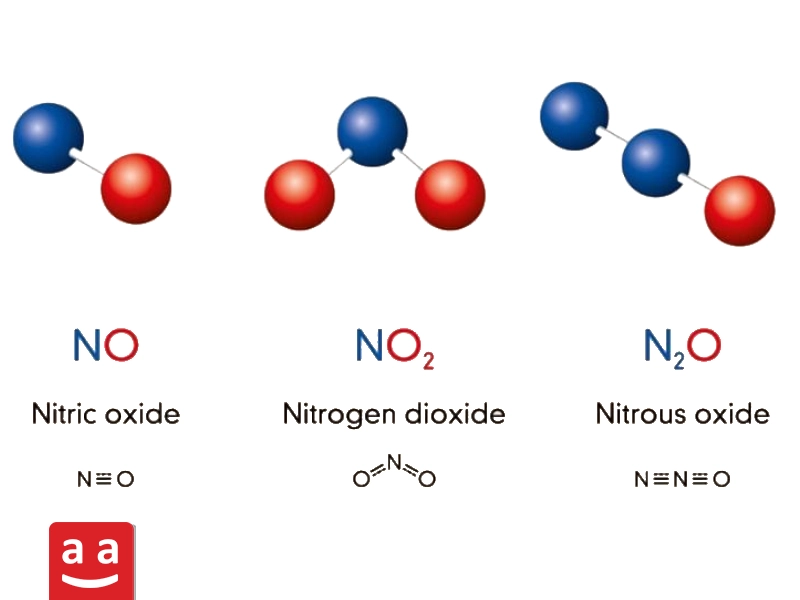

سه مکانیزم عمده در تشکیل اکسیدهای نیتروژن در واکنشهای احتراقی، مکانیزم ناکس حرارتی، مکانیزم ناکس فوری و مکانیزم ناکس سوختی است.
ناکس حرارتی عمدتاً در دماهای بالا و در حضور مقدار زیادی نیتروژن و اکسیژن تشکیل میشود. در این شرایط، مولکولهای نیتروژن در اثر گرمای زیاد به اجزای خود تجزیه شده و با اکسیژن ترکیب میشوند. این نوع ناکس در اغلب فرآیندهای احتراقی، بهویژه در تجهیزات صنعتی مانند بویلرها، توربینهای گازی و موتورهای احتراق داخلی، بیشترین سهم را دارد.
ناکس فوری ناشی از واکنش رادیکالهای آزاد تولیدشده در حین احتراق است. این واکنشها معمولاً در مراحل اولیه احتراق رخ داده و به تشکیل ترکیبات ناپایدار نیتروژنی منجر میشوند که به سرعت به اکسیدهای نیتروژن تبدیل میشوند.
ناکس سوختی زمانی ایجاد میشود که ترکیبات نیتروژن موجود در ساختار شیمیایی سوخت، در حین احتراق شکسته شده و اتمهای نیتروژن آزادشده با اکسیژن واکنش میدهند. این نوع ناکس بهویژه در سوختهای مایع و جامد، مانند نفت کوره و زغالسنگ، به میزان قابلتوجهی تولید میشود. مقدار آن به ترکیب شیمیایی سوخت، شرایط سوختن و دمای شعله بستگی دارد.
آلایندگی ناشی از کربن مونوکسید (CO)
کربن مونوکسید (CO) به طور کلی در تعداد کمی از فرآیندهای احتراق به عنوان محصول احتراق ناقص تولید میشود. کربن مونوکسید یک گاز قابل اشتعال است که بی رنگ، بی بو، بی مزه و معمولاً غیر خورنده است. کربن مونوکسید در تمام محصولات احتراقی که از سوختهای کربنی استفاده میکنند یافت میشود. در حالت تعادل کربن مونوکسید توسط معادله 8 تشکیل میشود.
معادله 8
CO2 → CO + 0.5O2
غلظت کربن مونوکسید به دما و هوای اضافی بستگی دارد. در ناحیه غنی از سوخت احتراق، سطح کربن مونوکسید به دلیل نبود اکسیژن کافی زیاد میشود. تنها در صورتی که هوای کافی با سوخت در دمای بالا مخلوط شود، مقدار کربن مونوکسید کاهش مییابد. در احتراق با میزان سوخت پایین، کربن مونوکسید در ترکیب با هوا به مولکولهای کربن دی اکسید تبدیل خواهد شد.
کربن مونوکسید بطور کلی در اثر سوختن ناقص یک سوخت هیدروکربنی تولید میشود. یک سیستم اشتعال در ناحیه فقیر از سوخت برای اطمینان از سوختن کامل و به حداقل رساندن انتشار کربن مونوکسید از اکسیژن اضافی استفاده میکند. شکل زیر نمودار نسبت هوا به سوخت در فرآیند احتراق و میزان انتشار آلاینده کربن مونوکسید را نشان میدهد. در این نمودار محور افقی بیانگر نسبت هوا به سوخت در فرآیند احتراق است. نسبت هوا به سوخت در حالت استوکیومتری برابر عدد یک در نظر گرفته شده است.
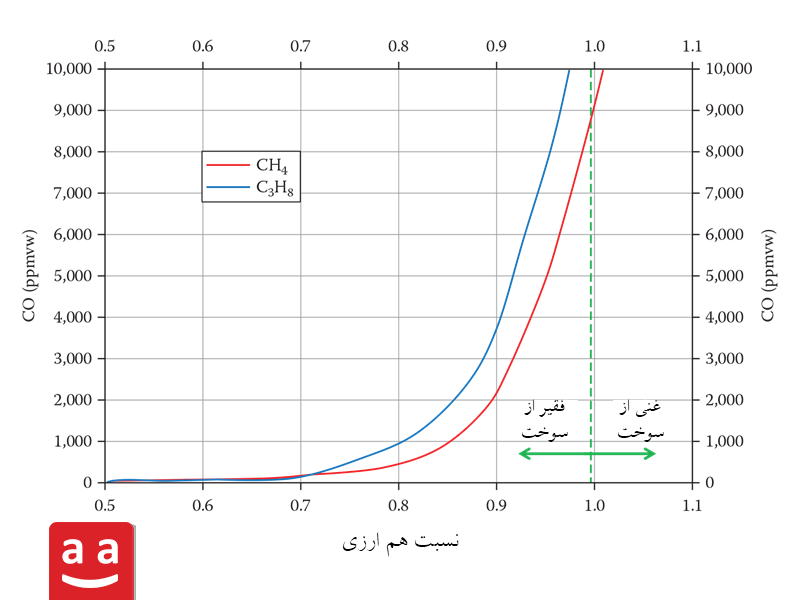

مشعلهای رادمن با طراحی مهندسی دقیق، قابلیت عملکرد با هوای اضافه پایین را دارند، که این ویژگی منجر به افزایش راندمان احتراق، کاهش تولید آلایندهها و بهینهسازی مصرف سوخت میشود. برای کنترل دقیق میزان هوای اضافه، میتوان از سنسورهای CO/O₂ Trim مانند سنسورهای شرکت AutoFlame استفاده کرد. این سیستمها به طور پیوسته مقدار اکسیژن و مونوکسید کربن موجود در گازهای خروجی را اندازهگیری کرده و به کمک یک کنترلر هوشمند، نسبت هوا به سوخت را تنظیم میکنند.
دمای آدیاباتیک شعله
در صورت عدم وجود تلفات حرارتی، دمای محصولات اشتعال به حداکثر میزان خود میرسد که به آن دمای آدیاباتیک شعله گویند. در شکل زیر دمای آدیاباتیک شعله برای سه سوخت هیدروژن، متان و پروپان بر حسب نسبت همارزی آورده شده است.
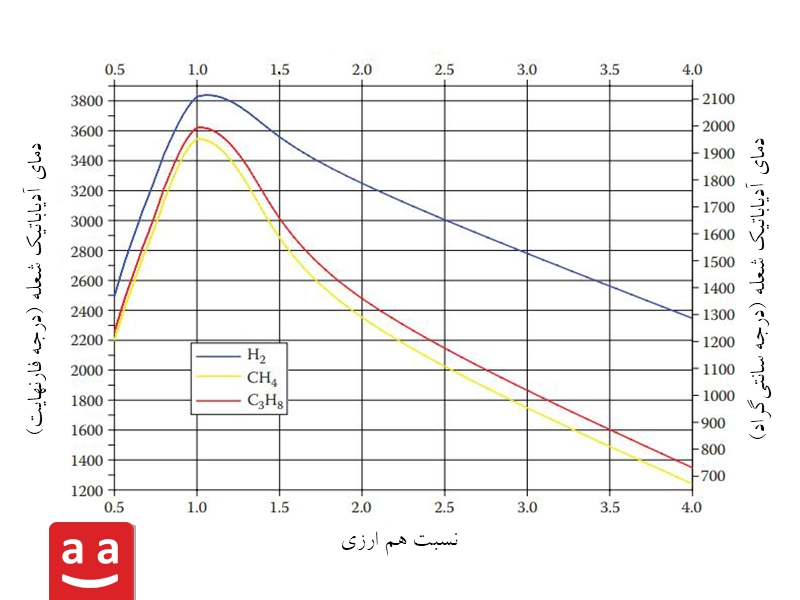

پیک دما (بیشینه دما) برای سوختها در شکل فوق در شرایط نزدیک به استوکیومتری رخ داده است. در بسیاری از شعلههای واقعی، بیشینه دما در شرایط سوخت رقیق رخ میدهد. علت آن جلوگیری از سوختن ناقص است و برای تکمیل احتراق نیاز به اکسیژن بیشتری است. تقریبا تمامی کاربردهای صنعتی در شرایط سوخت رقیق صورت میگیرند تا پایین بودن میزان کربن مونوکسید تضمین شود. بنابراین با توجه به طراحی واقعی مشعلها، دمای شعله میتواند به پیک دما (شرایطی که برای بیشینه کردن انتقال حرارت مطلوب است) نزدیک باشد.
بالاترین دمایی که توسط محفظه احتراق میتواند تحمل شود به جنس آن محفظه بستگی دارد. لذا دمای آدیاباتیک شعله عامل مهمی در طراحی محفظه احتراق توربینهای گاز، بویلرها و … است. در جدول 2، دمای شعله آدیاباتیک برای برخی سوختها آورده شده است.
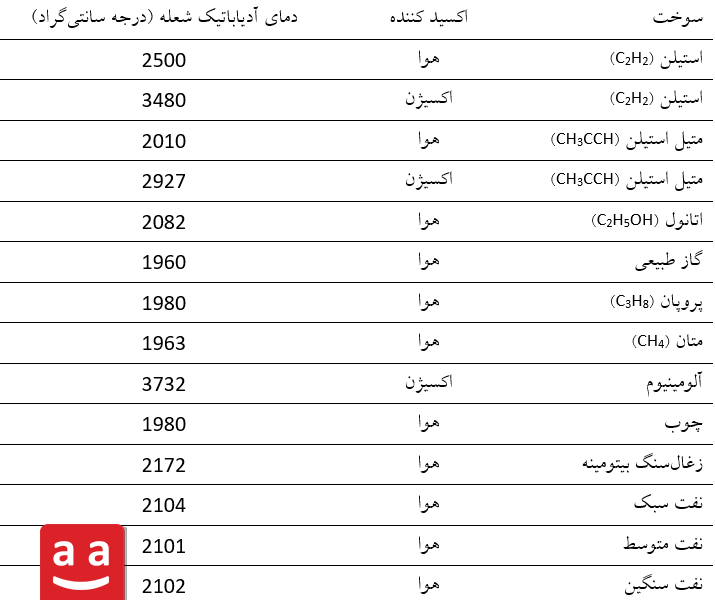

یکی از چالشهای اصلی در شعلههای با دمای بالا، مساله بیشینه شدن ناکس است. میزان تولید ناکس حرارتی بهصورت نمایی با افزایش دما رشد میکند، ازاینرو بسیاری از طراحیهای نوین بر کاهش دمای شعله بهمنظور حداقلسازی تولید ناکس متمرکز شدهاند. در این راستا، مشعلهای رادمن با طراحی پیشرفته خود، توزیع بهینه سوخت و هوا را به گونهای انجام میدهند که از ایجاد نواحی با دمای بیشینه جلوگیری کرده و در نتیجه، تولید ناکس را به حداقل میرسانند.
انواع احتراق
احتراق به دو صورت انجام میگیرد که در ادامه مورد بحث قرار گرفته است.
احتراق پیشآمیخته
در یک شعله پیشآمیخته همگن، سوخت و هوا ابتدا به صورت کامل با هم مخلوط شده و سپس با استفاده از یک عامل شروع واکنش مانند جرقه، اشتعال صورت میگیرد. از محل جرقه، شعله ایجاد شده و شروع به پیشروی میکند. سطح مشترک قسمتهای سوخته شده و سوخته نشده را جبهه یا پیشانی شعله میگویند. جبهه شعله با سرعت معینی به سمت قسمتهایی که درگیر واکنش نشدهاند، حرکت میکند که طی آن شدت احتراق بسیار بالا است.
احتراق پیشآمیخته در مشعلهای پیشمخلوط، از جمله مشعلهای پیشرفته رادمن، کاربرد دارد. این دسته از مشعلهای صنعتی بهگونهای طراحی شدهاند که در آنها سوخت و هوا پیش از ورود به سری احتراقی با یکدیگر ترکیب شده و سپس فرآیند سوختن در محل تشکیل شعله صورت میگیرد. این فناوری منجر به بازدهی بالاتر و کاهش چشمگیر آلایندههایی مانند CO و NOx میشود، که از مزایای کلیدی مشعلهای پیشمخلوط رادمن بهشمار میرود.


احتراق غیر پیش آمیخته
در یک شعله غیر پیشآمیخته واکنشهای پیش از سوختن قبل از ترکیب سوخت و اکسید کننده انجام میشود. پس از آن با ورود سوخت و هوا به محفظه احتراق و اختلاط آنها، اشتعال به شکل همزمان با نفوذ مولکولهای سوخت در اکسید کننده صورت میگیرد. شدت اشتعال در این نوع شعلهها تابع میزان اختلاط سوخت و اکسید کننده است. اشتعال در موتورهای دیزل، توربینهای گاز، شعله کبریت و شمع، مشعلهای کوره و … همگی از نوع غیر پیشآمیخته هستند.
احتراق غیر پیشآمیخته در مشعلهای نازل میکس کاربرد دارد. در این نوع مشعل، سوخت و هوا تا قبل از خروج از نازل، جدا از هم حرکت میکنند. هوا و سوخت تازه وقتی که به دهانهی نازل یا بعد از آن میرسند، با هم ترکیب میشوند و سوختن صورت میگیرد. پاکمن با دانش فنی بالا به طراحی و تولید مشعلهای نازل میکس مطابق استانداردهای ملی و بینالمللی میپردازد. مشعلهای رادمن با تمرکز بر کاهش آلایندهها و بهینهسازی مصرف انرژی طراحی میشوند و میتوانند فرآیندهای سوختن را در صنایع مختلف بهبود ببخشند.


سخن پایانی: احتراق بهینه با مشعلهای صنعتی پیشرفته
مشعلهای صنعتی نقش اساسی در بهینهسازی فرآیند سوختن و کاهش آلایندههای زیستمحیطی ایفا میکنند. درک اصول احتراق، از جمله نسبتهای استوکیومتری، دمای آدیاباتیک شعله و مکانیسمهای تشکیل آلایندههایی مانند ناکس و CO، برای طراحی سیستمهای احتراقی کارآمد ضروری است. کنترل دقیق میزان هوای اضافی و استفاده از فناوریهای نوین در طراحی مشعلها میتواند تأثیر مستقیمی بر افزایش راندمان سوختن و کاهش آلایندهها داشته باشد.
در این راستا، مشعلهای رادمن با طراحی پیشرفته خود، امکان اختلاط بهینه سوخت و هوا را فراهم کرده و علاوه بر افزایش بازدهی احتراق، به کاهش تولید آلایندههای زیستمحیطی کمک میکنند. این فناوری با کنترل بهتر دمای شعله و جلوگیری از ایجاد نواحی دمایی بیشینه، از تشکیل بیشازحد آلایندههایی مانند ناکس جلوگیری میکند. در نتیجه، بهرهگیری از دانش مهندسی و فناوریهای پیشرفته در طراحی مشعلها، راهکاری مؤثر برای کاهش اثرات مخرب زیستمحیطی و دستیابی به احتراقی بهینه و پایدار است.






