Оксиды азота являются одними из самых значимых и опасных загрязнителей, образующихся в результате процессов сгорания, и могут наносить серьезный ущерб окружающей среде и здоровью человека. В данной статье рассматриваются три основных механизма образования этих загрязняющих веществ, а именно: термические оксиды азота, топливные оксиды азота и быстрые оксиды азота. Также анализируются методы снижения выбросов этих веществ. Ввиду важности контроля за выбросами данных соединений, точное понимание этих механизмов может способствовать разработке эффективных стратегий по снижению загрязнения воздуха и улучшению качества окружающей среды. Среди технологий, способствующих снижению выбросов оксидов азота, можно выделить горелки
Что такое оксиды азота (NOx)?
Одним из нежелательных продуктов сгорания в промышленности являются оксиды азота, которые называются NOx. Эти соединения образуются в процессе сгорания и считаются одной из основных причин загрязнения воздуха в городах. NOx, благодаря своему участию в химических реакциях в атмосфере, могут вызывать экологические и медицинские проблемы. NOx — это общее название для семейства оксидов азота, которое включает семь различных химических соединений, перечисленных в таблице ниже.
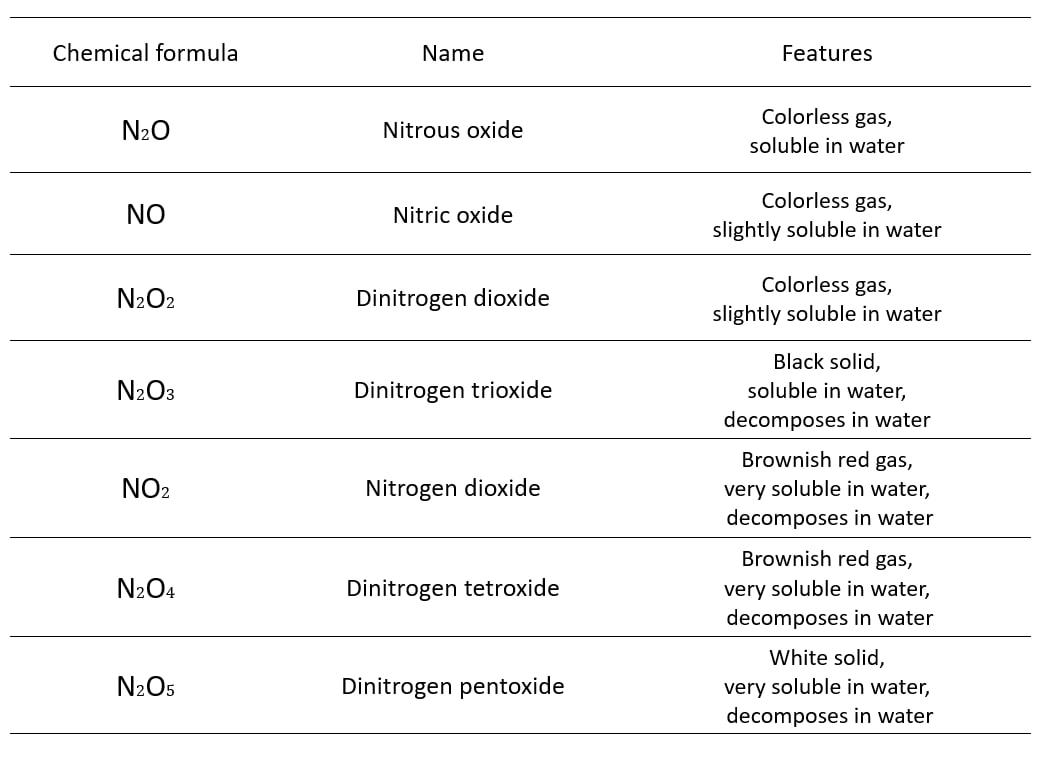
Среди семи вышеперечисленных химических соединений наиболее распространённой формой оксидов азота в атмосфере является NO₂ (диоксид азота). По этой причине Агентство по охране окружающей среды США (EPA) рассматривает этот молекулу как основной показатель загрязнения NOx. Когда речь идет о NOx в контексте сгорания, в первую очередь подразумеваются NO и NO₂. Хотя и другие формы оксидов азота могут образовываться в процессе сгорания, только NO и NO₂ выделяются в значительных количествах. Именно поэтому стандарты и нормативы устанавливаются для этих двух соединений. Следует отметить, что NO, образующийся при сгорании, в конечном итоге вступает в реакцию с кислородом и озоном в атмосфере, превращаясь в NO₂.
Характеристики оксидов азота
Оксид азота (NO)
Бесцветный и без запаха газ, образующийся при высоких температурах в процессах сгорания. Легко вступает в реакцию с кислородом, превращаясь в диоксид азота (NO₂).
Диоксид азота (NO₂)
Бурый газ с резким запахом, постоянно взаимодействующий с другими химическими соединениями в атмосфере, что приводит к образованию кислотных дождей и наземного озона.
Экологический ущерб
Присутствие оксидов азота в атмосфере может вызывать серьёзные экологические проблемы.
Образование кислотных дождей: Эти загрязнители реагируют с водой в атмосфере и образуют азотную кислоту (HNO₃), что приводит к разрушению городских сооружений, снижению качества сельскохозяйственных продуктов и ущербу для почвы и водных ресурсов.
Образование озона на уровне поверхности: В присутствии солнечного света и в сочетании с летучими углеводородами образуется озон (O₃) на уровне поверхности, который может вызывать респираторные проблемы и повреждения растительности.
Вред для здоровья человека: Вдыхание этих загрязнителей может вызывать раздражение дыхательных путей, повышать чувствительность к респираторным и сердечно-сосудистым заболеваниям, а также усугублять хронические болезни, такие как астма.
С учетом ущерба и рисков, связанных с оксидами азота, а также растущей чувствительности обществ к вопросам охраны окружающей среды, в настоящее время применяются строгие стандарты относительно этих загрязнителей, которые значительно ограничивают объемы выбросов NOx в промышленных предприятиях, автомобилях с внутренним сгоранием и т. д. Эти законы и стандарты способствовали успешному снижению концентрации оксидов азота в атмосфере многих индустриальных стран. Например, ниже представлена графика, показывающая изменение средней концентрации NOx в воздухе США с 1980 по 2023 год.
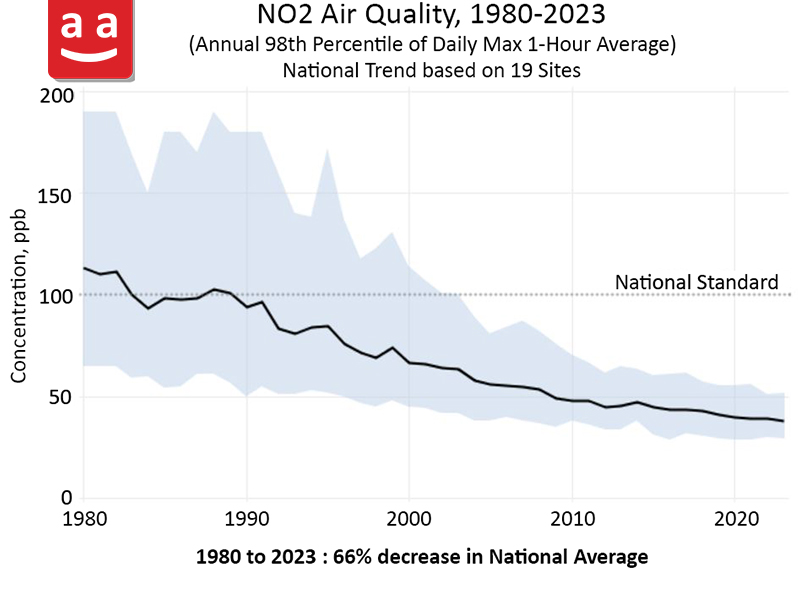
Примечание: В Иране также можно значительно снизить выбросы этих опасных загрязнителей, расширив использование существующих технологий для уменьшения оксидов азота, таких как предсмешанные горелки, горелки с низким уровнем NOx, системы рециркуляции продуктов сгорания РДГ (FGR), а также улучшив эффективность двигателей внутреннего сгорания.
Способ образования NOx
Образование оксидов азота в процессах сгорания, как правило, происходит через три основных механизма. Далее мы объясним каждый из этих механизмов.
1. Термический NOx (Thermal NOx)
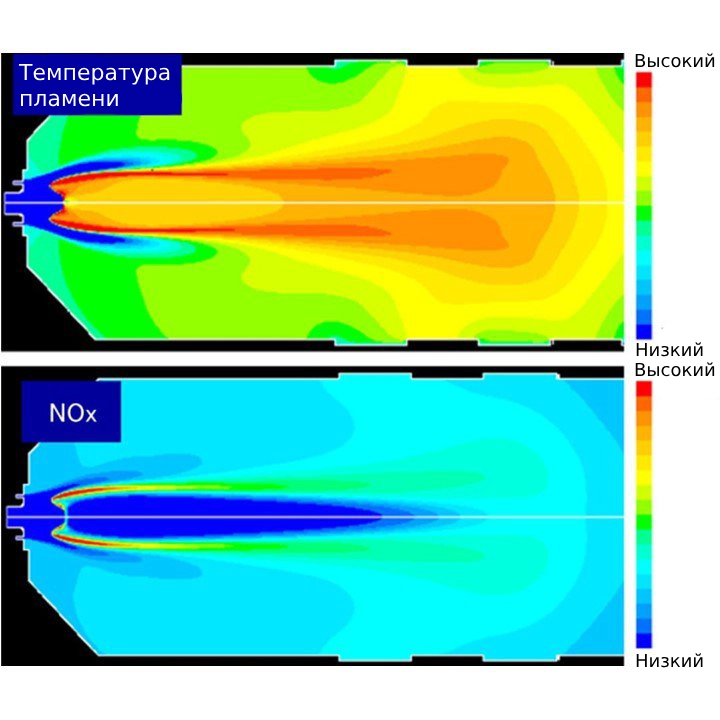
Этот тип оксидов азота образуется при очень высоких температурах, особенно в котлах и двигателях внутреннего сгорания. Химические реакции между азотом (N₂) и кислородом (O₂) при температурах выше 1300 градусов Цельсия приводят к разрушению связей этих элементов и образованию NO. Снижение температуры пламени и концентрации кислорода являются основными методами для уменьшения производства этого типа оксидов.
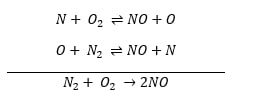
Этапы реакции:
- Первый этап: Один атом азота (N) сталкивается с молекулой кислорода (O₂). Результатом этого столкновения является образование молекулы оксида азота (NO) и одного атома кислорода (O). Эта реакция запускает цепочку реакций.
- Второй этап: Атом кислорода, образовавшийся на первом этапе, сталкивается с молекулой азота (N₂). Результатом этого столкновения является образование молекулы оксида азота (NO) и одного атома азота (N). Образованный атом азота снова вступает в реакцию на первом этапе, и эта цепочка продолжается.
Конечный результат:
Когда мы рассматриваем оба этапа вместе, результатом является то, что из реакции одной молекулы азота (N₂) с одной молекулой кислорода (O₂) образуются две молекулы оксида азота (NO).
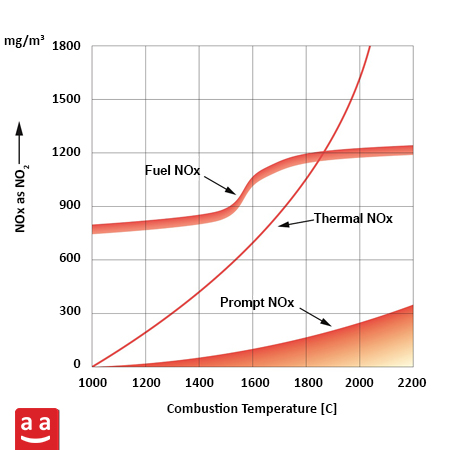
Как мы говорили в начале, эти реакции происходят при очень высоких температурах. Это связано с тем, что для того, чтобы молекулы азота и кислорода распались и образовали отдельные атомы, требуется много энергии. Высокая температура в пламени промышленных горелок обеспечивает необходимую энергию.
Молекула кислорода (O₂) с двойной связью расщепляется легче, чем молекула азота (N₂), у которой тройная связь. Это значит, что разрушение молекулы азота происходит труднее, и поэтому второй этап, где происходит это разрушение, является стадией, которая ограничивает скорость всей реакции. Проще говоря, так как второй этап медленнее, он определяет скорость всей реакции.
Уравнение изменения концентрации NO во время реакции: Предполагая, что атомарный кислород находится в равновесии с молекулярным кислородом, концентрация NO со временем изменяется по следующему уравнению:
NO=A[N2] ∫e(−b/T) [O2] dθNO = A[N₂] ∫e^{(-b/T)} \sqrt{[O₂]} dθNO=A[N2] ∫e(−b/T) [O2]dθ
NO: объемная концентрация оксида азота
N₂: объемная концентрация азота
O₂: объемная концентрация кислорода
T: абсолютная температура
θ: время
A и b: константы, зависящие от условий реакции.
Основные моменты:
- Влияние температуры: более высокая температура значительно увеличивает производство NO. Поэтому горячие точки внутри пламени, где температура выше, являются основными источниками NO. Следовательно, если мы сможем снизить температуру пламени, мы можем уменьшить производство NO.
- Влияние концентрации кислорода: Концентрация кислорода также играет важную роль в производстве NO. Чем выше концентрация кислорода в зоне реакции, тем больше образуется NO. Таким образом, уменьшив концентрацию кислорода, мы можем снизить производство NO.
- Постоянство концентрации азота: во время реакции концентрация азота практически не изменяется, и её можно считать почти постоянной. Поэтому влияние концентрации азота в уравнении представляется в виде постоянного коэффициента.
Стратегии уменьшения термических NOx
На основе этого уравнения и пояснений можно выделить три основных метода для уменьшения производства NOx в процессе сгорания:
- Снижение температуры пламени: так как температура сильно влияет на образование NOx, снижение температуры пламени является одним из самых эффективных способов уменьшения NOx.
- Снижение концентрации кислорода: Уменьшая количество кислорода в топливно-воздушной смеси, можно снизить производство NOx.
- Сокращение времени горения при высоких температурах: если мы сможем уменьшить время, в течение которого горение происходит при высоких температурах в присутствии кислорода, производство NOx также снизится.
Эти ключевые методы контроля и сокращения термических NOx могут способствовать улучшению качества воздуха и снижению загрязнения окружающей среды.
2. NOx, связанные с топливом (Fuel-Bound NOx)
Эти соединения образуются, когда азот, содержащийся в молекулах ископаемого или биотоплива, вступает в реакцию с кислородом. Топливо, такое как уголь и нефть, обычно содержит азот, который при высоких температурах превращается в оксиды азота (NOx). Использование более чистого топлива, например природного газа, может снизить образование этих загрязняющих веществ.
Роль молекулы азота (N₂) в топливе
Следует отметить, что, если топливо содержит только молекулы азота (N₂) в свободной форме, этот азот не может способствовать образованию NOx, связанных с топливом, и даже может способствовать их снижению. Фактически, молекулы азота (N₂), присутствующие в топливе в виде газа, из-за своей высокой химической стабильности не вступают в процесс горения и могут действовать как разбавитель. Этот разбавитель уменьшает концентрацию активных веществ в реакции и снижает температуру пламени, что, в свою очередь, уменьшает образование термических NOx и NOx, связанных с топливом.
Этапы образования:
- Первый этап: когда топливо, содержащее атомы азота (например, CxHyN), горит, оно сначала разлагается на промежуточные продукты, такие как HCN (цианистый водород) и CN (цианид). Этот этап показан в следующем уравнении:
CxHyN → HCN + CN + … - Второй этап: на следующем этапе эти промежуточные продукты вступают в реакцию с кислородом (O₂), в результате чего образуется оксид азота (NO). Этот процесс представлен в следующем уравнении:
HCN + CN + O₂ → NO + …
Как можно снизить образование NOx, связанных с топливом?
- Снижение концентрации кислорода: если концентрация кислорода в камере сгорания уменьшится, то и образование оксида азота, связанного с топливом, также снизится, так как скорость превращения промежуточных продуктов (HCN и CN) в оксид азота (NO) уменьшится.
- Использование топлива без азота: если использовать топливо, не содержащее азота, например природный газ, образование NOx, связанных с топливом, будет невозможно. Поэтому одним из эффективных способов снижения образования NOx в промышленности является использование топлива, не содержащего азот.
3. Быстрые оксиды азота (Prompt NOx)
В этом механизме азот, содержащийся в воздухе, непосредственно реагирует с молекулами топлива. Промежуточные вещества, образующиеся в результате этих реакций, превращаются в NO. Этот механизм может происходить при более низких температурах и обычно наблюдается, когда концентрация топлива в камере сгорания высокая. Разбавление топлива и снижение его концентрации в камере сгорания могут помочь уменьшить образование этого типа оксидов.
Этапы образования:
- Первый этап: на этом этапе молекулы топлива (например, CHx) реагируют с молекулами азота (N₂), присутствующими в воздухе. Эта реакция приводит к разрушению прочной тройной связи между атомами азота (N≡N) и образованию промежуточных продуктов, таких как HCN и CN. Этот этап более сложный по сравнению с образованием NOx, связанными с топливом, так как разрушение сильной связи между атомами азота требует больше энергии.
CHx + N₂ → HCN + CN + …
- Второй этап: на этом этапе промежуточные продукты (HCN и CN) реагируют с кислородом (O₂), в результате чего образуется оксид азота (NO).
HCN + O₂ → NO + …
Факторы, влияющие на образование быстрых NOx
- Концентрация топлива: чем выше концентрация топлива в камере сгорания, тем выше вероятность реакции с азотом и образования быстрых оксидов азота.
- Концентрация азота (N₂): поскольку азот в воздухе в большом количестве, снижение его концентрации обычно невозможно. Это означает, что акцент следует делать на снижении концентрации топлива.
Уменьшение образования быстрых NOx
Наилучший способ снижения образования быстрых оксидов азота — это разбавление топлива перед сгоранием. То есть, до того\, как топливо достигнет зоны пламени, его следует смешать с уже существующими продуктами сгорания в камере. Это можно сделать, проектируя горелку таким образом, чтобы высокоскоростные струи топлива захватывали и смешивались с продуктами сгорания. Таким образом, топливо разбавляется, и образование оксидов азота уменьшается.

Исследование современных технологий снижения NOx в различных отраслях
С развитием технологий и ростом экологических забот, различные отрасли стремятся уменьшить выбросы опасных загрязняющих веществ, таких как оксиды азота (NOx). NOx является одним из самых значительных загрязнителей городского воздуха, который наносит вред здоровью человека и экосистемам. В этой связи, современные технологии снижения NOx были предложены в качестве эффективных решений. Далее рассмотрим некоторые из этих технологий.

1. Системы рециркуляции продуктов сгорания (FGR)
Эта система снижает температуру пламени и предотвращает образование термических NOx путем возврата части отработанных газов сгорания обратно в камеру сгорания. Благодаря своей простоте и высокой эффективности, эта технология широко применяется в котлах и газовых турбинах.
2. Селективные каталитические редукторы (SCR)
Технология SCR является одним из наиболее эффективных методов снижения NOx, применяемых в энергетической и автомобильной отраслях. В этой системе аммиак или мочевина вводятся в выхлопные газы и, с помощью специализированных катализаторов, NOx преобразуются в безвредный азот и воду.
3. Прямое впрыскивание пара или воды
Впрыск пара или воды в камеру сгорания снижает температуру пламени и ограничивает образование термических NOx. Преимущество этого метода заключается в относительно низкой стоимости и возможности внедрения в уже существующие системы.
4. Горелка Premix с низким выбросом NOx
Горелка Premix, смешивая топливо и воздух до сгорания, снижают температуру пламени и образование NOx. В таких горелках благодаря равномерному распределению температуры пламени образуется значительно меньше термических NOx.
5. Горелки с низким выбросом NOx
Горелки с низким выбросом NOx с особой конструкцией камеры сгорания обеспечивают создание пламени с равномерной температурой. Эти горелки значительно снижают выбросы оксидов азота (NOx) за счет понижения температуры пламени. Технология широко используется в котлах и промышленных печах.
6. Ступенчатый процесс сгорания (Staging Combustion)
При таком процессе сгорания топливо или воздух вводятся поэтапно, что снижает скорость реакции и предотвращает образование пламени с высокой температурой. Это позволяет значительно сократить выбросы NOx. Такой тип сгорания широко используется в горелках энергетической отрасли и в нефтехимической промышленности.
7. Искусственный интеллект и цифровое моделирование
Одной из последних инноваций является использование искусственного интеллекта и компьютерного моделирования для оптимизации процесса сгорания и снижения NOx. Этот метод помогает предприятиям анализировать данные и моделировать различные условия, что позволяет найти наилучшие настройки сгорания.
8. Использование чистых топлив
Переход от ископаемых топлив к чистым, таким как природный газ или биотопливо, может значительно снизить производство NOx. Это изменение, в сочетании с технологиями снижения NOx, играет важную роль в уменьшении загрязнения воздуха.
Способы улучшения качества воздуха через снижение NOx
Учитывая негативные последствия этих загрязняющих веществ для общественного здоровья и окружающей среды, необходимо разработать новые стратегии и технологии для контроля и уменьшения их производства. Использование более чистого топлива — один из методов снижения выбросов оксидов азота. Оптимизация процессов сгорания также может уменьшить образование этих загрязняющих веществ. Применение современных технологий, таких как предварительно смешанные горелки и системы рециркуляции продуктов сгорания (FGR), также эффективно снижает выбросы оксидов азота. Эти меры могут способствовать улучшению работы систем сгорания.
В Иране также можно значительно снизить выбросы этих опасных соединений и улучшить качество воздуха, расширив использование существующих технологий и улучшив работу двигателей сгорания.
Использование более чистых видов топлива, оптимизация процессов сгорания и внедрение технологий снижения NOx, таких как горелки с низким уровнем NOx и предварительно смешанные горелки Радман, системы рециркуляции продуктов сгорания (FGR) и другие, могут помочь снизить уровень выбросов NOx в различных системах сгорания.







